১৮৮৭ সালে অম্ল-ক্ষারকের আরহেনিয়াস মতবাদ প্রকাশিত হবার ৩৬ বছর পর ১৯২৩ সালে দৃশ্যপটে যৌথভাবে হাজির হলেন দুই নতুন মুখ – জার্মান বিজ্ঞানী নিকোলাস ব্রনস্টেড এবং ইংরেজ রসায়নবিদ টমাস লাউরি। তারা প্রদান করলেন অম্ল-ক্ষারকের নতুন তত্ত্ব (Brønsted-Lowry Theory of Acids and Bases)
অম্ল আর ক্ষারককে ব্রনস্টেড-লাউরি নতুনভাবে সংজ্ঞায়িত করলেন এভাবে –
- অম্ল হল প্রোটন (proton) বা হাইড্রোজেন আয়ন (H+) দাতা
- ক্ষারক হল প্রোটন (proton) বা হাইড্রোজেন আয়ন (H+) গ্রহীতা
প্রোটন আদান-প্রদানকে ভিত্তি করে অম্ল ক্ষারককে পরিচয় করিয়ে দেয় বলে এই মতবাদকে অম্ল ক্ষারকের প্রোটনীয় মতবাদ বলেও অভিহিত করা হয়।
অনেকের মনে হতে পারে, ব্রনস্টেড-লাউরি এর এই প্রস্তাবনাগুলো বুঝি আরহেনিয়াস মতবাদের সাথে সংঘাত সৃষ্টি করছে। বস্তুত, এই প্রোটনীয় মতবাদ আরহেনিয়াস মতবাদের বিরুদ্ধে তো যায়ই না, উল্টো তার পরিপূর্ণতা সাধন করে।
তাহলে আমাদের পরিচিত অম্ল আর ক্ষারকগুলো এবং তাদের মধ্যে ঘটা প্রশমন বিক্রিয়াকে এই মতবাদের প্রেক্ষিতে নতুনভাবে আবিষ্কার করা যাক? 😀
প্রথমে আসি অম্লের ব্যাপারে। অম্লের যে সংজ্ঞা আরহেনিয়াস রেখে গিয়েছিলেন তার সাথে ব্রনস্টেড-লাউরির অম্লের সংজ্ঞার পার্থক্য যৎসামান্য। কিন্তু সূক্ষ্ম পার্থক্যটা হল, আরহেনিয়াস বলেছিলেন – অম্ল তারাই যারা জলীয় দ্রবণে হাইড্রোজেন আয়ন (H+) দান করতে পারে। তো এই হাইড্রোজেন আয়ন বা প্রোটন দ্রবণে কীভাবে থাকে তা সম্পর্কে কোনো সুস্পষ্ট ব্যাখ্যা তিনি দিয়ে যান নি। ব্রনস্টেড ও লাউরির সাফল্য হল, তারা কেবল অম্লকে প্রোটন দাতা বলেই সীমাবদ্ধ থাকলেন না; সাথে এটাও উল্লেখ করলেন প্রোটনটা মুক্ত না থেকে একটা গ্রহীতা দ্বারা গৃহীত হবে। এই যে প্রোটন গ্রহীতা আমাদের, সে-ই হল ক্ষারক। ব্যাপারখানি অনেকটা এমন – বিজারক ইলেকট্রন ছাড়লেই যেমন সেই ইলেকট্রন মুক্ত না থেকে জারক কর্তৃক গৃহীত হয়; তেমন করে প্রোটনও অম্ল থেকে ছাড়া পেয়ে তৎক্ষণাৎ খুঁজে নেয় ক্ষারককে।
পুরো ঘটনাটার সুন্দর একটা উদাহরণ হতে পারে পানিতে HCl এর বিযোজন প্রক্রিয়া। এই বিক্রিয়াটাকে আরহেনিয়াসের প্রকল্প অনুসারে আমরা এভাবে দেখে এসেছি –
HCl (g) + H2O (l) → H+ (aq) + Cl– (aq)
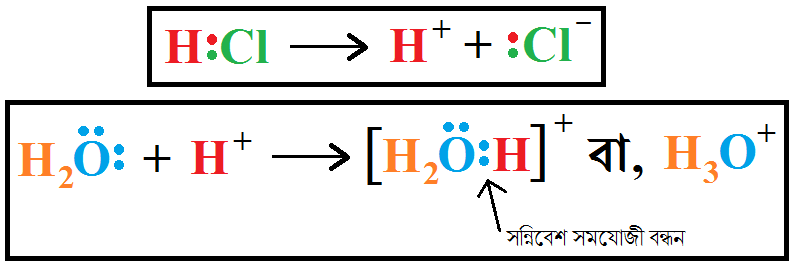
কিন্তু ব্রনস্টেড-লাউরির মতে এই ছেড়ে দেওয়া হাইড্রোজেন আয়নকে (H+) পানির অণু (H2O) ক্ষারক হিসেবে গ্রহণ করবে। পানির অণুতে থাকা দু’টি মুক্ত ইলেকট্রন জোড়ের একটি জোড় আগত প্রোটনের সাথে সন্নিবেশ সমযোজী বন্ধন তৈরি করে ও তদানুসারে জন্ম নেয় হাইড্রোনিয়াম আয়ন বা হাইড্রোক্সোনিয়াম আয়ন (H3O+)। তাহলে এখানে নতুন এবং বিস্ময়কর দু’টি ব্যাপার আমরা লক্ষ্য করি – ১. ব্রনস্টেড এবং লাউরি অম্লের বিযোজন দেখাতে গিয়ে দ্রাবক পানিকে ক্ষারক বানিয়ে দিলেন! এবং ২. HCl থেকে দ্রবণে আসা প্রোটন তাহলে সাথেসাথেই ক্ষারকের OH– এর সাথে বিক্রিয়া করে পানি বানিয়ে ফেলতে পারছে না, তাকে অপেক্ষা করতে হচ্ছে H3O+ আয়ন আকারে যে আয়ন গঠনের কথা পূর্বের আরহেনিয়াস মতবাদে উল্লেখ ছিল না।
সুতরাং প্রকৃতভাবে বিক্রিয়াটাকে লেখা উচিত এরকম করে –
HCl (aq) + H2O (l) → H3O+ (aq) + Cl– (aq)
চিত্র আকারে দেখি এই এসিড বিয়োজনের সম্পূর্ণ ঘটনাটা –
এবার ধরা যাক, এই অম্লের দ্রবণে আমরা NaOH এর জলীয় দ্রবণ যোগ করলাম। এই জলীয় দ্রবণে কী কী আছে সেটা আমাদের জানা দরকার। NaOH আয়নিত হয়ে সোডিয়াম আয়ন ও হাইড্রোক্সাইড আয়ন তৈরি করে থাকে – এটা আমরা জানি। তাহলে NaOH তো একটা ক্ষারক, তাই না?
উঁহু! ভুল হয়ে যাচ্ছে! ভুলে যাওয়া চলবে না যে এখানে প্রোটনীয় মতবাদ নিয়ে আলোচনা চলছে। এই মতবাদ অনুযায়ী কেউ প্রোটন গ্রহন করলে তবেই তাকে ক্ষারক বলা যাবে, অন্যথায় নয়। NaOH, OH– দান করে বলে আরহেনিয়াস মতবাদ অনুযায়ী সে ক্ষারক হতে পারে, কিন্তু প্রোটনীয় চিন্তাধারায় যতক্ষণ না একে প্রোটন গ্রহন করতে দেখছি ততক্ষণ পর্যন্ত এর গায়ে ক্ষারকের সিল দিতে আমরা রাজী নই।
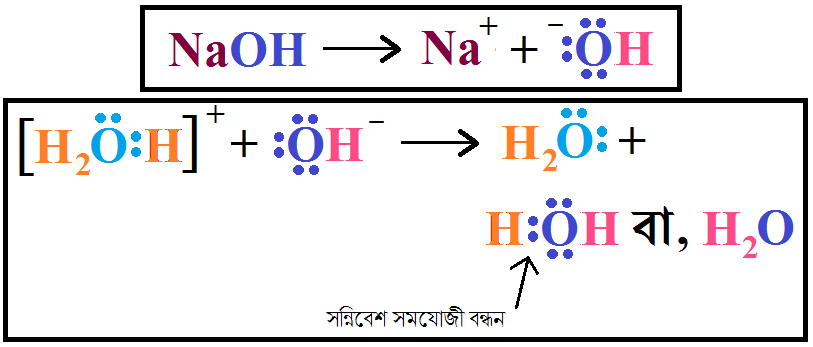
আবার ফিরে যাই NaOH দ্রবণ HCl দ্রবণে যোগ করার মুহূর্তে। দুই দ্রবণ পর যোগ করার পর মিশ্রণে থাকা OH– আয়ন দেখবে H3O+ খুব মাস্তানি করে বেশি বেশি হাইড্রোজেন নিয়ে ঘুরছে। সাম্য প্রতিষ্ঠা করতে H3O+ থেকে তখনই প্রোটন বের হয়ে যাবে এবং পুনরায় সন্নিবেশ সমযোজী বন্ধন তৈরি করে যুক্ত হতে থাকবে OH– আয়নের সাথে; উৎপন্ন হবে পানির অণু। ওদিকে H3O+ ও প্রোটন বিসর্জন দিয়ে পানি হবে বৈকি! এটাই তো আমাদের প্রশমন বিক্রিয়া, যাতে পানি তৈরি হচ্ছে! 😀
প্রশমন বিক্রিয়া তো দেখলাম, এখন? এখন পাগলামি করে আমি যা লিখব সেটা দেখে তোমার হৃদযন্ত্র বন্ধ হলেও হতে পারে। উদ্ভট সেই তথ্যগুলো হচ্ছে –
এই প্রশমন বিক্রিয়ায় NaOH প্রকৃতভাবে ক্ষারক নয় এবং প্রশমন বিক্রিয়াটিতে HCl অম্ল হিসেবে কাজ করে না।
সত্যিই দেখ, একদম শেষে লেখা বিক্রিয়াটায়, যেখানে প্রশম উৎপাদ পানি উৎপন্ন হচ্ছে, সেখানে কি তোমার প্রিয় NaOH কে খুঁজে পাচ্ছ? অথবা পাচ্ছ খুঁজে অম্ল অম্ল বলে হম্বিতম্বি করা HCl কে? উত্তর হল, না!
আসলে এই প্রশমন বিক্রিয়ায় পানি তৈরির সময় HCl নিজে অম্ল হিসেবে কাজ করে না, অম্লের কাজ করে H3O+ আয়ন যে আগেই প্রোটন বুঝে নেয় HCl এর কাছ থেকে। একইভাবে আস্ত NaOH অণুর কোনো প্রয়োজন নেই এই বিক্রিয়া ঘটাতে। OH– আয়নই শুধু গ্রহন করে প্রোটনটা, অর্থাৎ ঐ বিক্রিয়ায় হাইড্রোক্সাইড আয়নই আমাদের প্রোটনগ্রাহী ক্ষারক।
একটু বেশিই বলে ফেললাম বুঝি 😛 জেনে রাখো, এসবের মানে এই না যে HCl এবং এর মত আরও যাদের অম্ল বলে তুমি চিনে এসেছ (H2SO4, H3PO4, HNO3, CH3COOH) তারা আর অম্ল রইল না। এরা যদি প্রথমেই এসিড হিসেবে প্রোটন না দিত পানিকে, তবে H3O+ এর কি সাধ্য হত ক্ষারককে প্রশমিত করার? আর NaOH ও তার মত অন্যরা (NaOH, KOH, Ca(OH)2) যদি না থাকত, তাহলে OH– ই বা তুমি পেতে কোথা থেকে আর ক্ষারক হিসেবে প্রোটনই বা নিত কে? তাই আরহেনিয়াস মতবাদে বলা এই অম্ল-ক্ষারকগুলো একশবার অম্ল আর ক্ষারক হিসেবে টিকে থাকবে! প্রথমেই বলেছিলাম না? প্রোটনীয় মতবাদ আরহেনিয়াস মতবাদকে বাতিল করতে আসে নি, এসেছে আরো সূক্ষ্ম পর্যবেক্ষণ উপস্থাপন করে এই মতবাদকে পরিপূর্ণ করতে।
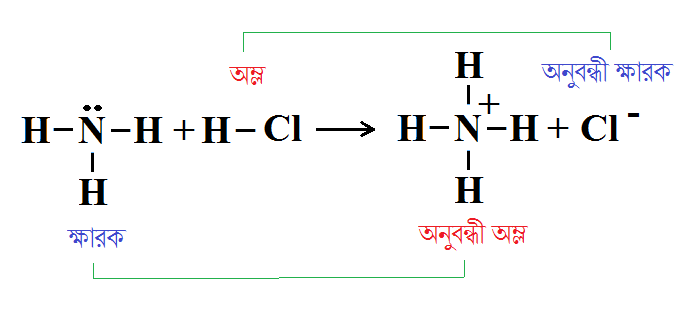
গত পর্বে আমরা একটা ঝামেলায় পড়েছিলাম না গ্যাসীয় অ্যামোনিয়া আর হাইড্রোজেন ক্লোরাইড গ্যাসের মধ্যে বিক্রিয়ায় কীভাবে অ্যামোনিয়াম ক্লোরাইড লবণ তৈরি হতে পারে তা নিয়ে? এই বিক্রিয়াটার ব্যাখ্যাও উপস্থাপন করা যায় ব্রনস্টেড-লাউরির মতবাদ দিয়ে। NH3 এর কেন্দ্রীয় পরমাণু নাইট্রোজেন সন্নিবেশ সমযোজী বন্ধন তৈরি করে HCl থেকে প্রোটন গ্রহন করে এবং ফলশ্রুতিতে তৈরি হয় NH4+ ও Cl– আয়ন।
এই আমোনিয়া পানিতে দ্রবীভূত হলেও ক্ষারধর্মীতার পানির কাছ থেকে প্রোটন নেয় ও অ্যামোনিয়াম আয়ন তৈরি করে, প্রোটন হারানো সেই পানি হয়ে যায় হাইড্রোক্সাইড আয়ন (পানি এখানে এসিডের মত কাজ করে) –
NH3 (g) + H2O (l) → NH4+ (aq) + OH– (aq)
এখন যদি এই ক্ষারীয় দ্রবণে তুমি কোনো এসিড দ্রবণ যোগ কর তবে কী কী ঘটবে তা নিশ্চয়ই তোমার আর অজানা নয় 😀
অনুবন্ধী অম্ল-ক্ষারক যুগল (Conjugate pair)
HCl এর পানিতে বিযোজন আবার স্মরণ কর –
HCl (aq) + H2O (l) → H3O+ (aq) + Cl– (aq)
সমীকরণের বামপক্ষে স্পষ্টতই HCl হল অম্ল এবং তার কাছ থেকে প্রোটন গ্রহণের অপেক্ষায় থাকা H2O হল ক্ষারক।
এই বিক্রিয়াটাকে আমরা একমুখী হিসেবে লিখেছি, কিন্তু এসকল বিক্রিয়া কখনো সম্পূর্ণভাবে একমুখী নয়। HCl বেশ সবল এসিড বলে তা প্রায় শতভাগ আয়নিত হয় ও পানিকে প্রোটন উপহার দেয়। কিন্তু বিপরীতমুখী বিক্রিয়াকে আমলে নিলে এমনটাও তো হওয়া সম্ভব – পানির অণু প্রোটন গ্রহন করে যে H3O+ তৈরি করেছিল তা Cl– কে প্রোটন দিয়ে আবার H2O আর HCl তৈরি করল।
তারমানে এখানে উৎপাদ হিসেবে যে H3O+ আছে, তার সামর্থ্য তৈরি হয়েছে প্রোটন দিয়ে এসিডের মত বিক্রিয়া দেবার। ক্ষারক H2O এর প্রোটন গ্রহনের ফলে এই যে প্রোটন দানে সক্ষম এক সত্তার উৎপত্তি ঘটেছে, এই রাসায়নিক সত্তাকে আমরা বলি অনুবন্ধী অম্ল। অন্যদিকে HCl ছিল এসিড, তা প্রোটন হারিয়ে যে Cl– তৈরি করেছে তা পুনরায় প্রোটন গ্রহন করে ক্ষারকের মত বিক্রিয়া দিতে পারঙ্গম। এটিকে তাই বলা যাবে অনুবন্ধী ক্ষারক।
সুতরাং, যেকোনো অম্ল-ক্ষারক বিক্রিয়ায় অম্ল প্রোটন হারিয়ে তৈরি করে তার অনুবন্ধী ক্ষারক আর ক্ষারক প্রোটন গ্রহন করে উৎপন্ন করে অনুবন্ধী অম্ল। এসব বিক্রিয়াগুলোয় সর্বদা দুইজোড়া অনুবন্ধী অম্ল-ক্ষারক পাওয়া যায়।
সেই অ্যামোনিয়া আর হাইড্রোজেন ক্লোরাইডের বিক্রিয়া থেকেও আমরা খুঁজে নিতে পারি অনুবন্ধী অম্ল ক্ষারকের যুগলগুলো।
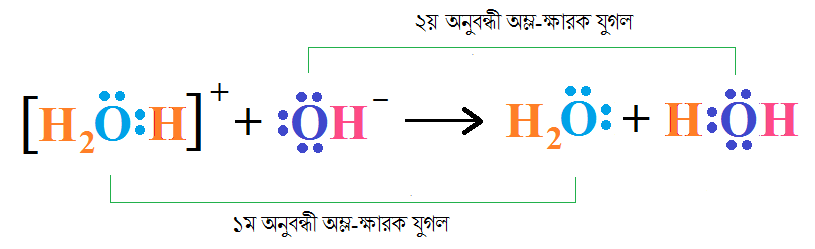
H3O+ আর OH– এর বিক্রিয়াটাই বা আর বাদ রাখি কেন?
একটা অম্ল যত শক্তিশালী হয় তার অনুবন্ধী ক্ষারক তত দুর্বল হয়। এর কারণ হল অম্ল শক্তিশালী হলে তার বিয়োজন হয় দ্রুত, তা খুবই স্বতঃস্ফূর্তভাবে ক্ষারককে প্রোটন দিয়ে দিতে পারে। সম্মুখবর্তী বিক্রিয়ায় অধিক সক্রিয় অম্ল হতে প্রোটন চলে গিয়ে স্থিতিশীল অনুবন্ধী ক্ষারক তৈরি হয়। একটা স্থিতিশীল সুস্থির জিনিস থেকে অস্থিতিশীল ও সক্রিয় জিনিস তো তৈরি হতে চায় না। প্রকৃতির নিয়মই হল স্থিতিশীলতা অর্জন ও সুস্থিত হওয়া। তাই ঐ ক্ষারক পুনরায় প্রোটন গ্রহনে আর আগ্রহী হয় না। আর প্রোটন গ্রহনে অনিচ্ছুক এমন কোনো ক্ষারককে তুমি নিশ্চয়ই শক্তিশালী ক্ষারকের খেতাব দিতে চাইবে না; ক্ষারকের প্রোটন গ্রহনে সক্রিয়তাই যে তার সবলতার সূচক।
উপরের কথাগুলো সুন্দরমত খাটে অজৈব বা খনিজ এসিডগুলোর জন্য (HCl, H2SO4, H3PO4, HNO3) । জৈব এসিড যেমন ইথানয়িক এসিডের (CH3COOH ) জন্য ব্যাপারটা উল্টো। এই এসিড দুর্বল কেননা তা বিয়োজনের পরে যে ইথানয়েট আয়ন (CH3COO–) উৎপন্ন হয় তা স্থিতিশীল নয়, এটি প্রোটন গ্রহন করে ইথানয়িক এসিড রূপে থাকতেই বেশি পছন্দ করে। তাই বেচারা এসিড প্রোটন ছাড়তে বেশ বেগ পায় এবং দ্রবণে প্রায় অবিয়োজিত অবস্থায় থাকে। সুতরাং আমরা রায় দিতে পারি – দুর্বল অম্লের অনুবন্ধী ক্ষারক সবল হয়। একইভাবে সবল ক্ষারকের অনুবন্ধী অম্ল দুর্বল (OH–, H2O) এবং দুর্বল ক্ষারকের অনুবন্ধী অম্ল সবল (NH3, NH4+) হয়ে থাকে।
অনুবন্ধী যুগলগুলোর এই স্থিতিশীলতা/সক্রিয়তা তুলনা করে এসিড/ক্ষারকের তীব্র বা দুর্বল হওয়ার কারণ ব্যাখ্যা প্রোটনীয় মতবাদ দ্বারাই সম্ভব, যা আরহেনিয়াস মতবাদ ইতোপূর্বে আমাদের নিকট উপস্থাপন করতে পারে নি।
অ্যাম্ফিপ্রোটিক ও অ্যাম্ফোটেরিক যৌগ (Amphiprotic & Amphoteric Compounds)
অ্যাম্ফিপ্রোটিক যৌগ সেসব পদার্থ যারা প্রোটন গ্রহন বা বর্জন – দু’টিই করতে পারে। H2O এমন যৌগের আদর্শ উদাহরণ। কারণ তা প্রোটন গ্রহন করে যেমন H3O+ হতে পারে, তেমন প্রোটন বর্জন করে OH–ও উৎপন্ন করতে পারে। প্রোটন গ্রহনের সময় পানি ক্ষারক আর বর্জনের সময় এসিড হিসেবে কাজ করবে। এরকম আরো উদাহরণ হল HCO3– (প্রোটন গ্রহনে H2CO3, প্রোটন দানে CO32-), CH3COOH (জলীয় দ্রবণে অতি সামান্য আয়নিত হয় প্রোটন ত্যাগ করে, CH3COO– ; তীব্র এসিডের উপস্থিতিতে প্রোটন গ্রহনও করতে পারে কিটো মূলকে থাকা অক্সিজেনের সাথে সন্নিবেশ বন্ধন তৈরি করে, CH3COOH2+ )
অন্যদিকে অ্যাম্ফোটেরিক যৌগ তারাই যারা অম্ল আর ক্ষার উভয়ের মত বিক্রিয়া দিতে পারে। এ কথা বলার অপেক্ষা রাখে না, অ্যাম্ফিপ্রোটিক পদার্থ মাত্রই অ্যাম্ফোটেরিক পদার্থ কারণ অ্যাম্ফিপ্রোটিক পদার্থগুলো প্রোটন গ্রহন বর্জনের উপর ভিত্তি করে ক্ষারক কিংবা অম্ল হতে পারে। কিন্তু অম্ল ক্ষারক উভয় হলেই যে অ্যাম্ফিপ্রোটিক হতে হবে এমন কোনো কথা নেই। বলা যায়, অ্যাম্ফোটেরিক যৌগের একটা টাইপ হল অ্যাম্ফিপ্রোটিক যৌগ।
অ্যাম্ফোটেরিক কিন্তু অ্যাম্ফিপ্রোটিক নয় এমন যৌগের উদাহরণ হল উভধর্মী অক্সাইডগুলো (Al2O3, ZnO) যারা অম্ল ক্ষারক উভয়ের সাথেই বিক্রিয়া করতে পারে –
Al2O3 + 6HCl → 2AlCl3 + 6H2O (এখানে Al2O3 ক্ষারক)
Al2O3 + 2NaOH → 2NaAlO2 + H2O (এখানে Al2O3 অম্ল)
এ পর্বে এতটুকুই 😀 পরবর্তী পর্বে আমাদের জন্য অপেক্ষা করছে অম্ল ক্ষারকের লুইস মতবাদ।
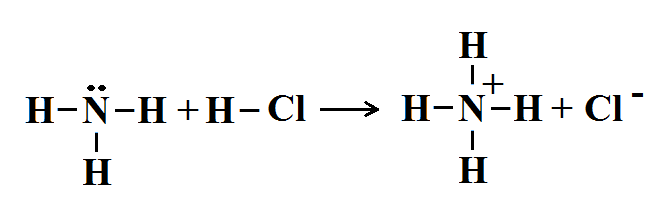
Change my concept totally ???? just speechless
ধন্যবাদ 😀
THANKS A LOT
তোমাকেও ধন্যবাদ 😀