গত পর্বে বলেছিলাম পরের পোস্ট হবে গাণিতিক সমস্যা নিয়ে। তা নিয়েই করছি শেষের শুরু।
প্রথম সমস্যাটা দেখ।
প্রথমেই আমরা লিখে ফেলি লবণটার বিযোজনের বিক্রিয়া।
এই বিযোজন থেকে তাহলে আমরা জানি যে ক্যালসিয়াম কার্বনেটের 1 litre সম্পৃক্ত দ্রবণ নিয়ে থাকলে তাতে S mol করে ক্যালসিয়াম আয়ন ও কার্বনেট আয়ন আছে। তাহলে আমরা এই সম্পৃক্ত দ্রবণের জন্য Ksp এর মানও বের করতে পারব এভাবে,
কিন্তু সমস্যা হচ্ছে এখানে S এর যে মান প্রশ্নে দেওয়া আছে তা বসিয়ে অংক করলে হবে না। S চাই mol/L এককে, g/L এ নয়।
হ্যাঁ, এবার Ksp এর মান এই S থেকে বের করা যাবে।
শেষ 😀 😀
এবার যাই দ্বিতীয় সমস্যায়।
এবার Ksp দেওয়া আছে, বের করব দ্রাব্যতা। চটজলদি Ksp এর সাথে S এর সম্পর্ক প্রতিষ্ঠা করে ফেলা যাক।
ব্যস, পরের পথটুকু এমন হওয়া উচিত।
কিন্তু প্রশ্নে কেবল এটাই চায় নি। চেয়েছে সম্পৃক্ত দ্রবণে বেরিয়াম ও ফ্লোরাইড আয়নের ঘনমাত্রাও। সম্পৃক্ত দ্রবণে প্রতি লিটারে S mol বেরিয়াম ফ্লোরাইড লবণ থাকে যা থেকে S mol বেরিয়াম আয়ন আর 2S mol ফ্লোরাইড আয়ন উৎপন্ন হয়, তাই নয় কি? তাহলে S জানলে এভাবেই বের করে ফেলা যায় এই দুই আয়নের ঘনমাত্রাও।
শেষ দ্বিতীয় সমস্যাও 😀 তৃতীয় সমস্যায় প্রবেশ করার আগে জেনে নিতে হবে আরেকটা জিনিস সম্পর্কে। তা হল কোনো দ্রবণের আয়নিক গুণফল (Ionic Product)।
দ্রবণের আয়নিক গুণফল বলতে কী বোঝায় দেখ : “নির্দিষ্ট তাপমাত্রায় কোনো আয়নিক যৌগের দ্রবণে ঐ যৌগের সংগঠক আয়নসমূহের যথোপযুক্ত ঘাতসহ মোলার ঘনমাত্রার গুণফলকে ঐ তাপমাত্রায় যৌগটির আয়নিক গুণফল বলে”।
এবার আবার রিপিট করি দ্রাব্যতা গুণফল এর সংজ্ঞাটা : “নির্দিষ্ট তাপমাত্রায় কোনো আয়নিক যৌগের সম্পৃক্ত দ্রবণে ঐ যৌগের সংগঠক আয়নসমূহের যথোপযুক্ত ঘাতসহ মোলার ঘনমাত্রার গুণফলকে ঐ তাপমাত্রায় যৌগটির দ্রাব্যতা গুণফল বলে”।
কোনো পার্থক্য খুঁজে পেলে? পার্থ্যক্যটা হল আয়নিক গুণফলের সংজ্ঞায় “সম্পৃক্ত” কথাটা বাদ গেছে। অর্থাৎ আয়নিক যৌগের যেকোনো দ্রবণের ক্ষেত্রে আয়নিক গুণফল বের করা যায়। দ্রবণ যখন সম্পৃক্ত হয়, তখনই আয়নিক গুণফলের নতুন নাম “দ্রাব্যতা গুণফল” দিই আমরা। আয়নিক গুণফল বের করা যায় ঠিক দ্রাব্যতা গুণফলের মত করেই, সংজ্ঞা আমাদের তো সেটাই শেখায় 😀
আয়নিক গুণফলকে Qsp দ্বারা প্রকাশ করা যায়। এই Qsp এর সাথে Ksp এর তুলনা করে সহজেই আমরা বলে দিতে পারি দ্রবণ এখন কোন অবস্থায় বিরাজ করছে। নিচের ছবিটা দেখ।
অর্থাৎ, Qsp , Ksp কে অতিক্রম করার অর্থই হল বাড়তি যে পরিমাণ আয়নগুলো দ্রবণে আছে, তা তলানি হিসেবে পড়বে 😀
এবার দেখা যাক তৃতীয় সমস্যাটা কী বলে।
তোমাকে লেড ক্লোরাইডের Ksp দিয়ে দিয়েছে এখানে, তারমানে ওরা চায় মিক্সিং এর পর যে লেড ক্লোরাইড উৎপন্ন হবে তার জন্য Qsp এর মান নির্ণয়পূর্বক তুমি তুলনা করে ওদের বলে দাও অধঃক্ষেপ পড়বে কি পড়বে না।
এখানে আরেকটা জিনিস বোঝানোর আছে, সেটা হল দুই দ্রবণের মিশ্রণ ঘটার পর লেড আয়ন আর ক্লোরাইড আয়নের ঘনমাত্রা কিন্তু একই থাকবে না। প্রথমে আয়তন V ছিল, পরে সময়ায়তন অন্য দ্রবণ যোগে আয়তন হয়ে গেল 2V, যার কারণে এদের ঘনমাত্রাতেও এল পরিবর্তন। আমরা ঐ ফাইনাল দ্রবণে এই আয়নগুলোর ঘনমাত্রা নির্ণয় করতে আগ্রহী। নিচের ছবিটাতে লেড আয়নের জন্য আমরা সেটা করে ফেলি। আয়তন পরিবর্তনের সাপেক্ষে ঘনমাত্রা বা মোলারিটির পরিবর্তনসংক্রান্ত এই সূত্র তো তোমরা জানই।
অনুরূপভাবে ক্লোরাইড আয়নের জন্য,
এবার? এবার এই দুই আয়ন একত্রে অবস্থান করছে একই পাত্রে। এদের জন্য আয়নিক গুণফল বের করে দ্রাব্যতা গুণফলের সাথে মেলান যাক।
Ksp এর মান ছিল 1.7 x 10-5 যা অপেক্ষা এই মান কম। তাই অধঃক্ষেপ পড়বে না 😀
এসে গেছি শেষ পর্যায়ে। তার আগে আরও একটা সমস্যা। আমরা কমন আয়ন ইফেক্ট নিয়ে অনেক কথা শুনেছি না? শুনেছি না একই দ্রবণে আগে থেকে কোনো নির্দিষ্ট আয়ন উপস্থিত থাকলে পরে ঐ আয়নধারী কেউ আর বিয়োজিত হতে চায় না? দেখে নাও দ্রাব্যতা দিয়েই এর চাক্ষুষ উদাহরণ।
হেহে! পানিতে দ্রাব্যতা নির্ণয় করতে দিয়েছে। Ksp দেওয়া থাকলে এটা কোনো ব্যাপার?
কিন্তু কিন্তু!! ঐ সোডিয়াম সালফেট দ্রবণে? তাতে তো আগে থেকেই সালফেট আয়ন আছে। তুমি একটা লবণ যেখানেই নাও না কেন, তার তাপমাত্রা ঠিক থাকলে Ksp কখনই চেঞ্জ হয় না। তবে কি বেরিয়াম সালফেটেরে দ্রাব্যতা কি আগের মতই হবে? আচ্ছা, ধরে নাও এর দ্রাব্যতা ঐ দ্রবণে S। তাহলে দ্রাব্যতা গুণফল নির্ণয় করার জন্য আমরা আবার সমীকরণ লিখি। এই সমীকরণে সালফেটের ঘনমাত্রা বসানোর সময় আমাদের একটু যত্নশীল হতে হবে কেননা কিছু সালফেট (0.1 M ঘনমাত্রার) আগেই থাকায় মিশ্রনে সালফেটের ঘনমাত্রা হয়ে যাবে (S+0.1)।
S এর মান অতি ক্ষুদ্র বলে আমরা (0.1+S) কে কেবল 0.1 ধরতে পারি আর তারপর এভাবে বের করতে পারি S এর মান –
পানিতে দ্রাব্যতার সাথে এই দ্রাব্যতা মিলিয়ে দেখ, এই দ্রাব্যতা প্রায় দশ হাজার গুণ কম!!! এভাবেই সমআয়ন বা কমন আয়ন প্রভাব সত্যিই প্রভাব ফেলে কোনো কিছুর দ্রাব্যতায় 😀
শেষ করছি এখানেই। আরো কিছু জানার কিংবা বলার থাকলে কমেন্ট করবে। সবাই পড়াশোনায় আরো দ্রবণীয় হবে এই কামনা করছি 😛

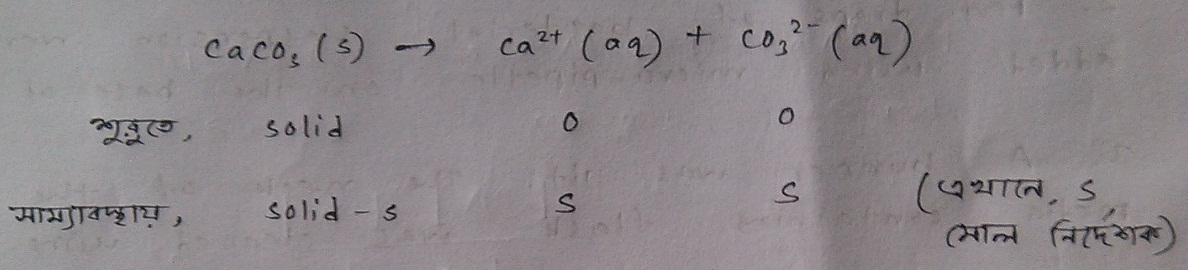
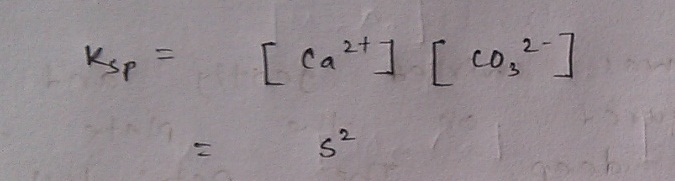
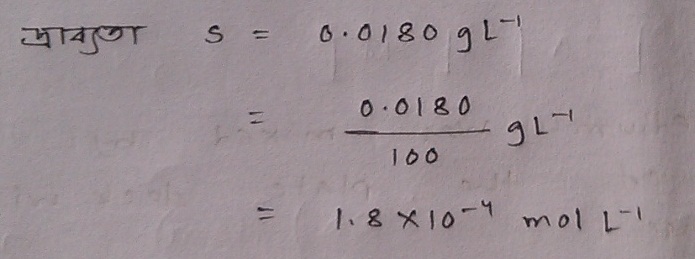
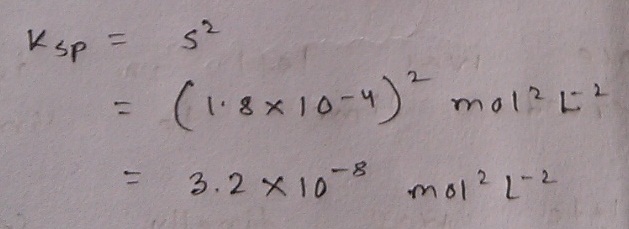

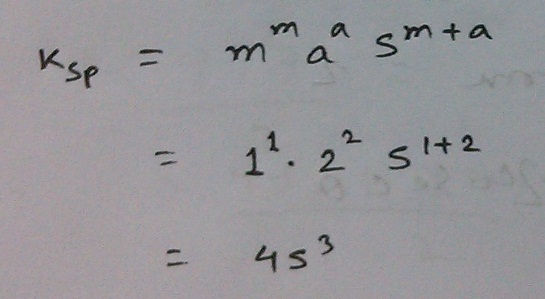



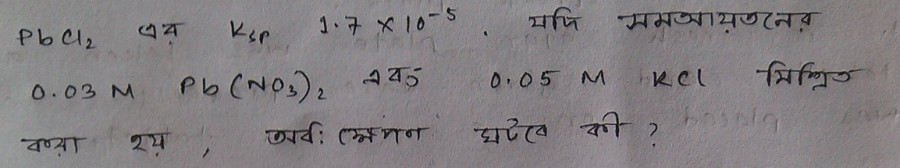
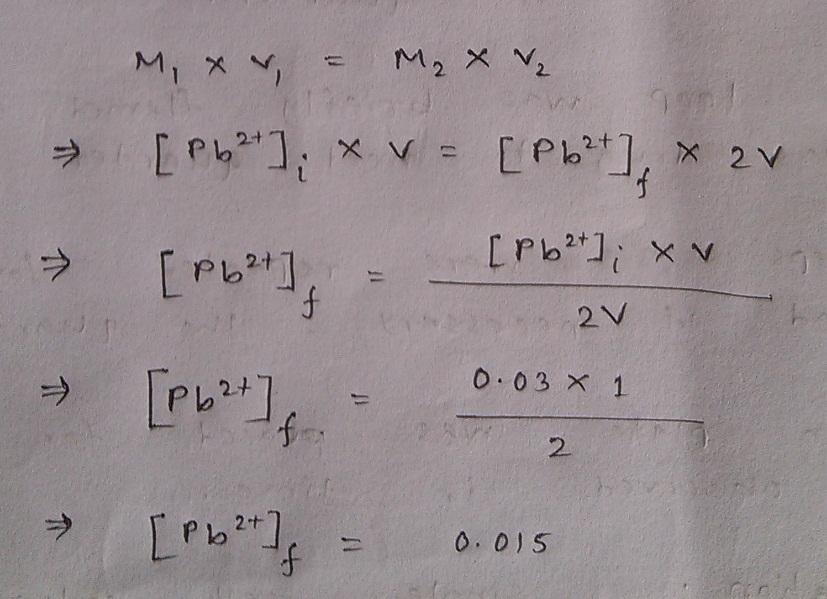
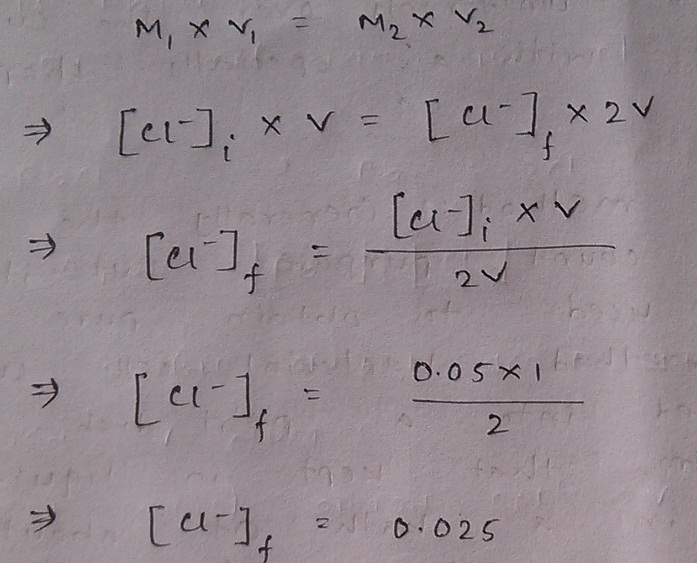
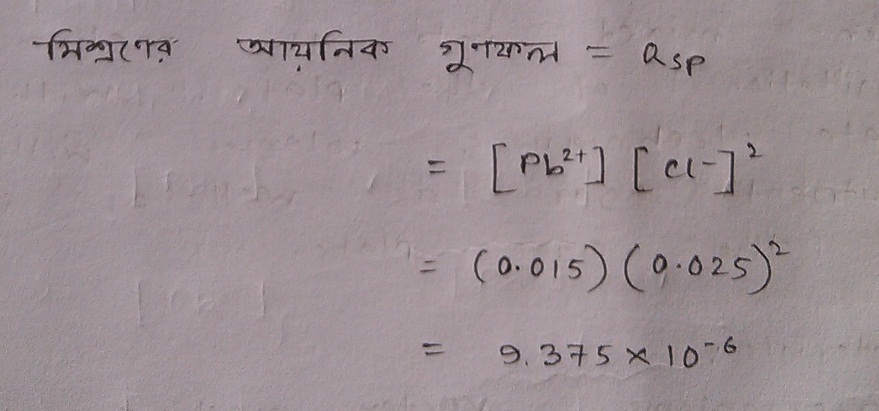

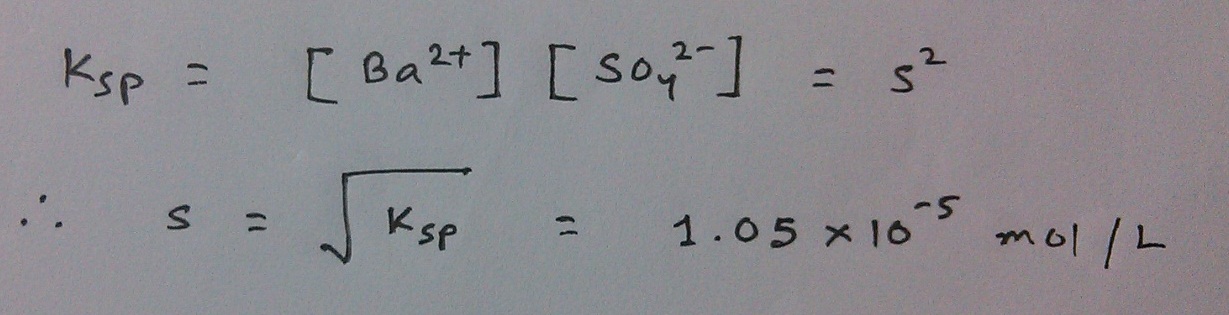
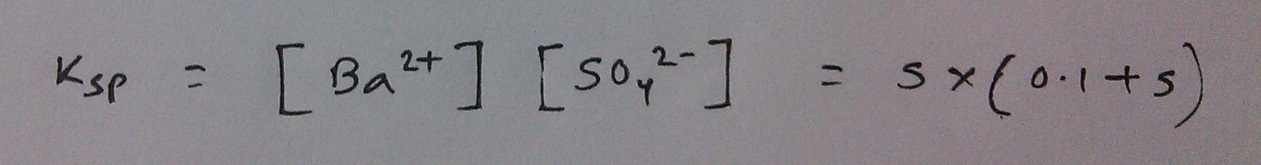

Joss ! Thanks ! Onk helpful ! Emon aro onk post chai ! Onk thanks !
ধন্যবাদ
Oshadharon…thanks.
ধন্যবাদ 😀
bhai, jinishgula english eo korle hoina
Bro! Where are you now? Need more.